мқҙлҹ° кё°мӮ¬
м–ҙл•Ңмҡ”?
мӢӨмӢңк°„
л№ лҘёлүҙмҠӨ
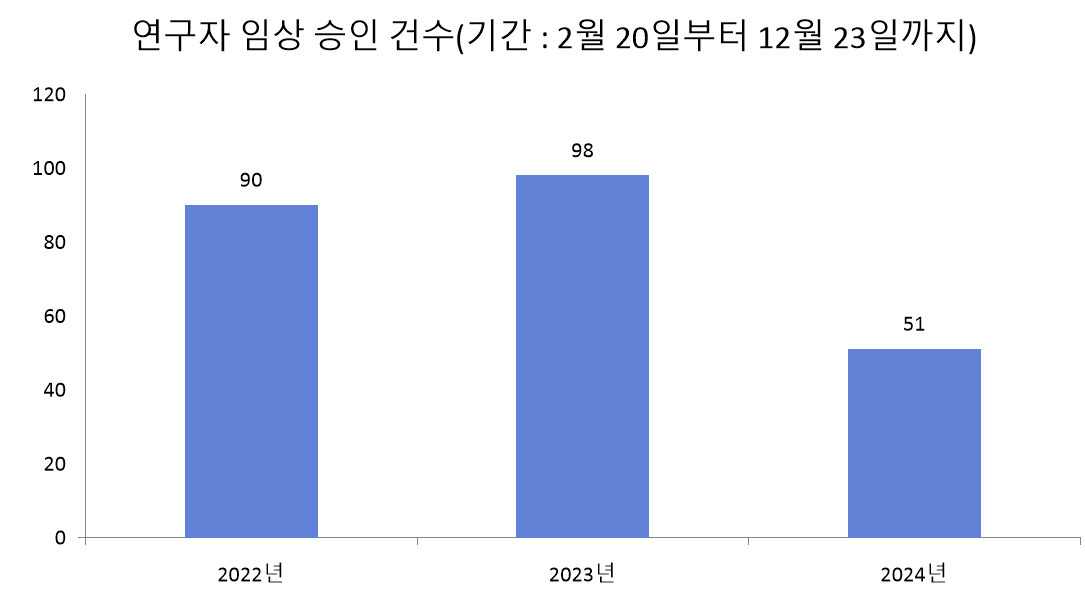
GCл…№мӢӯмһҗмӣ°л№ҷ, 'лӘЁл°ң кұҙк°• мң мӮ°к· ' мӢқм•ҪмІҳ мҠ№мқё
GCл…№мӢӯмһҗмӣ°л№ҷмқҖ мӢқн’Ҳмқҳм•Ҫн’Ҳм•Ҳм „мІҳлЎңл¶Җн„° 'лқҪнӢёлқҪнҶ л°”мӢӨлҹ¬мҠӨ м»ӨлІ нҲ¬мҠӨ(Latilactobacillus curvatus) LB-P9'лҘј лӘЁл°ң мғҒнғң(мңӨкё°·нғ„л Ҙ) к°ңм„ м—җ лҸ„мӣҖмқ„ мӨ„ мҲҳ мһҲлҠ” к°ңлі„мқём •нҳ• мӣҗлЈҢлЎң мҠ№мқёл°ӣм•ҳлӢӨкі 21мқј л°қнҳ”лӢӨ. LB-P9мқҖ м§ҖлӮң 2022л…„ мӢқн’Ҳмқҳм•Ҫн’Ҳм•Ҳм „мІҳм—җм„ң 'лӘЁл°ң кұҙк°•'мқ„ кұҙк°•кё°лҠҘмӢқн’Ҳ кё°лҠҘм„ұ лІ”мң„лЎң нҸ¬н•ЁмӢңнӮЁ нӣ„ көӯлӮҙ мөңмҙҲ мң мӮ°к· мңјлЎң лӘЁл°ңкұҙк°• кҙҖлҰ¬к°Җ к°ҖлҠҘн•ң кё°лҠҘм„ұ мң мӮ°к· мңјлЎң мҠ№мқёмқ„ л°ӣмқҖ к°ңлі„ мқём •нҳ• мӣҗлЈҢмқҙлӢӨ. нҠ№нһҲ, GCл…№мӢӯмһҗмӣ°л№ҷмқҖ мқҙлІҲ мӢқн’Ҳмқҳм•Ҫн’Ҳм•Ҳм „мІҳ мҠ№мқё мқҙнӣ„ мқёлҸҷлҚ©көҙкҪғлҙүмҳӨлҰ¬ 추м¶ңл¬ј, кө¬м ҲмҙҲ 추м¶ңл¬јм—җ
лҸҷм•„мҸҳмӢңмҳӨк·ёлЈ№, мӮ¬лһ‘мқҳ к№ҖмһҘ лӮҳлҲ” лҙүмӮ¬нҷңлҸҷ 진н–ү
лҸҷм•„мҸҳмӢңмҳӨк·ёлЈ№мқҖ мӢ мһ…мӮ¬мӣҗ 60м—¬ лӘ…мқҙ м§ҖлӮң 20мқј кІҪмғҒл¶ҒлҸ„ мғҒмЈјмӢңм—җ мң„м№ҳн•ң лҸҷм•„мҸҳмӢңмҳӨк·ёлЈ№ мқёмһ¬к°ңл°ңмӣҗм—җм„ң мӮ¬лһ‘мқҳ к№ҖмһҘ лӮҳлҲ” лҙүмӮ¬нҷңлҸҷмқ„ 진н–үн–ҲлӢӨкі 21мқј л°қнҳ”лӢӨ. м§ҖлӮңн•ҙ м—°л§җ к№ҖмһҘмӢңмҰҢ 배추 к°’ нҸӯл“ұмңјлЎң к№ҖмһҘ к№Җм№ҳ кө¬л№„м—җ м–ҙл ӨмӣҖмқ„ кІӘмқҖ мҶҢмҷёкі„мёөмқ„ мң„н•ҙ мӢ мһ…мӮ¬мӣҗл“ӨмқҖ к№ҖмһҘ к№Җм№ҳлҘј лІ„л¬ҙлҰ¬кі нҸ¬мһҘн•ҙ м·Ём•Ҫкі„мёө 250к°Җкө¬м—җ м „лӢ¬н–ҲлӢӨ. мқҙлІҲ лӮҳлҲ” н–үмӮ¬лҠ” лҸҷм•„мҸҳмӢңмҳӨк·ёлЈ№мқҳ м •лҸ„кІҪмҳҒ мӢӨмІңмқ„ мң„н•ң мӮ¬нҡҢкіөн—Ң н”„лЎңк·ёлһЁмқҳ мқјнҷҳмңјлЎң 진н–үн–ҲлӢӨ. н–үмӮ¬ м°ём—¬лЎң мӢ мһ…мӮ¬мӣҗл“ӨмқҖ кё°м—…мқҳ мӮ¬нҡҢм Ғ мұ…мһ„мқ„ лӘёмҶҢ мӢӨмІңн•ҳкі лӮҳлҲ”мқ„ нҶөн•ң л°°л Өмқҳ м •мӢ мқ„ лӮҳлҲ„лҠ” мӢңк°„мқ„ к°ҖмЎҢлӢӨ. н–үмӮ¬м—җлҠ” мғҒ
м „л¶ҒлҢҖлі‘мӣҗ л°©мӮ¬м„ мӮ¬ ліҙкұҙмқҳлЈҢ л°ңм „ кіөлЎң н‘ңм°Ҫ
м „л¶ҒлҢҖн•ҷкөҗлі‘мӣҗ мҳҒмғҒмқҳн•ҷкіј л°©мӮ¬м„ мӮ¬ 3лӘ…мқҙ м§Җм—ӯмӮ¬нҡҢ ліҙкұҙмқҳлЈҢ л°ңм „ кіөлЎңлҘј мқём •л°ӣм•„ м „л¶ҒнҠ№лі„мһҗм№ҳлҸ„ нҡҢмһҘмғҒ л°Ҹ көӯнҡҢмқҳмӣҗ н‘ңм°Ҫмқ„ л°ӣм•ҳлӢӨ. м „л¶ҒлҢҖлі‘мӣҗм—җ л”°лҘҙл©ҙ мөңк·ј к°ңмөңлҗң лҢҖн•ңл°©мӮ¬м„ мӮ¬нҳ‘нҡҢ м ң60нҡҢ м •кё°мҙқнҡҢм—җм„ң м „л¶ҒлҢҖлі‘мӣҗ мҳҒмғҒмқҳн•ҷкіј м •нғңмҳҒ·мөңмҡ©кұҙ л°©мӮ¬м„ мӮ¬к°Җ көӯлҜјліҙкұҙ н–ҘмғҒкіј л°ңм „м—җ кё°м—¬н•ң кіөлЎңлҘј мқём •л°ӣм•„ м „л¶ҒнҠ№лі„мһҗм№ҳлҸ„ нҡҢмһҘмғҒмқ„ л°ӣм•ҳлӢӨ. лҳҗ мқҙмһ¬м„қ л°©мӮ¬м„ мӮ¬лҠ” м§Җм—ӯмӮ¬нҡҢ ліҙкұҙмқҳлЈҢ л°ңм „мқҳ кіөлЎңлҘј мқём •л°ӣм•„ н•ңлі‘лҸ„ көӯнҡҢмқҳмӣҗмңјлЎңл¶Җн„° н‘ңм°Ҫмқ„ мҲҳм—¬л°ӣм•ҳлӢӨ. 2013л…„ м „л¶ҒлҢҖлі‘мӣҗ мҳҒмғҒмқҳн•ҷкіјм—җм„ң к·јл¬ҙлҘј мӢңмһ‘н•ң м •нғңмҳҒ, мөңмҡ©кұҙ л°©мӮ¬м„ мӮ¬лҠ” м§ҖлӮң 2023л…„м—җ
-
м „лӮЁлҢҖлі‘мӣҗ, көӯк°ҖнҶөн•© л°”мқҙмҳӨл№…лҚ°мқҙн„° кө¬м¶•мӮ¬м—… м„ м •
м „лӮЁлҢҖн•ҷкөҗлі‘мӣҗмқҖ мөңк·ј ліҙкұҙліөм§Җл¶ҖмҷҖ н•ңкөӯліҙкұҙмӮ°м—…진нқҘмӣҗмқҙ мЈјкҙҖн•ҳлҠ” 'көӯк°ҖнҶөн•© л°”мқҙмҳӨл№…лҚ°мқҙн„° кө¬м¶•мӮ¬м—…'м—җ м„ м •лҗҗлӢӨкі л°қнҳ”лӢӨ. көӯк°ҖнҶөн•© л°”мқҙмҳӨл№…лҚ°мқҙн„° кө¬м¶•мӮ¬м—…мқҖ көӯлҜј 'нҶөн•© л°”мқҙмҳӨ л№…лҚ°мқҙн„°'лҘј кө¬м¶•н•ҳкё° мң„н•ң көӯк°Җ мЈјлҸ„ м—°кө¬к°ңл°ң мӮ¬м—…мқҙлӢӨ. м°ём—¬мһҗлЎңл¶Җн„° нҳҲм•Ў, мҶҢліҖ, мЎ°м§Ғ л“ұмқҳ
-
"көӯлӮҙ мқҳлЈҢмӮ°м—… мңЎм„ұ"вҖҰмқҳлЈҢкё°кё°мӮ°м—…кі„-лі‘мӣҗкі„, нҳ‘л Ҙ к°•нҷ”
н•ңкөӯмқҳлЈҢкё°кё°мӮ°м—…нҳ‘нҡҢ(нҡҢмһҘ к№ҖмҳҒлҜј)лҠ” лҢҖн•ңлі‘мӣҗнҳ‘нҡҢ(нҡҢмһҘ мқҙм„ұк·ң)мҷҖ мөңк·ј лҢҖн•ңлі‘мӣҗнҳ‘нҡҢ мҶҢнҡҢмқҳмӢӨм—җм„ң көӯлӮҙ мқҳлЈҢмӮ°м—… мңЎм„ұкіј л°ңм „мқ„ мң„н•ң м—…л¬ҙнҳ‘м•Ҫ(MOU)мқ„ мІҙкІ°н–ҲлӢӨкі 21мқј л°қнҳ”лӢӨ. мқҙлІҲ нҳ‘м•ҪмқҖ мқҳлЈҢкё°кё° кё°м—…кіј лі‘мӣҗмқҙ м „мӢң·нҷҚліҙ нҳ‘л Ҙмқ„ нҶөн•ҙ көӯлӮҙ мқҳлЈҢмӮ°м—…мқҳ л°ңм „мқ„
-
мҳ¬лҰјн‘ёмҠӨн•ңкөӯ, м•” кІҪн—ҳмһҗ мҶҢнҶө 'кі мһү мҳЁ нҶ нҒ¬' м„ұлЈҢ
мҳ¬лҰјн‘ёмҠӨн•ңкөӯ(лҢҖн‘ң мҳӨм№ҙлӢӨ лӮҳмҳӨнӮӨ)мқҖ лҢҖн•ңм•”нҳ‘нҡҢ(нҡҢмһҘ мқҙлҜјнҳҒ)мҷҖ н•Ёк»ҳ м•” кІҪн—ҳмһҗ нҒ¬лҰ¬м—җмқҙн„°мқҳ мқҙм•јкё°лҘј лӮҳлҲ„лҠ” 'кі мһү мҳЁ нҶ нҒ¬(Going-on Talk)'лҘј м„ұнҷ©лҰ¬м—җ к°ңмөңн–ҲлӢӨкі 21мқј л°қнҳ”лӢӨ. кі мһү мҳЁ нҶ нҒ¬лҠ” м•” кІҪн—ҳмһҗм—җ лҢҖн•ң м •м„ңм Ғ м§Җм§ҖмҷҖ мӮ¬нҡҢм Ғ кіөк°җлҢҖ нҳ•м„ұмқ„ мң„н•ң мҳ¬лҰј
-
л©”л“ңнҠёлЎңлӢүмҪ”лҰ¬м•„, 'лҢҖн•ңлҜјкөӯ мқјн•ҳкё° мўӢмқҖ 100лҢҖ кё°м—…' 6л…„ м—°мҶҚ м„ м •
л©”л“ңнҠёлЎңлӢүмҪ”лҰ¬м•„к°Җ кёҖлЎңлІҢ м»Ём„ӨнҢ… кё°кҙҖ Great Place to Work Institute(мқҙн•ҳ GPTW)к°Җ нҸүк°Җ л°Ҹ л°ңн‘ңн•ҳлҠ” 'лҢҖн•ңлҜјкөӯ мқјн•ҳкё° мўӢмқҖ кё°м—…'м—җ 6л…„ м—°мҶҚ м„ м •лҗҗлӢӨкі 21мқј л°қнҳ”лӢӨ. л©”л“ңнҠёлЎңлӢүмҪ”лҰ¬м•„лҠ” 2025 GPTW м–ҙмӣҢмҰҲм—җм„ң лҢҖн•ңлҜјкөӯ мқјн•ҳкё° мўӢмқҖ 10
лӢ№мӢ мқҙ
мқҪмқҖ분야
мЈјмҡ”кё°мӮ¬
 м№ҙм№ҙмҳӨмұ„л„җ추к°Җ
м№ҙм№ҙмҳӨмұ„л„җ추к°Җ
















![[нҳ„мһҘ] '2024 м„ёкі„ л°”мқҙмҳӨ м„ңл°Ӣ' мқёмІңм„ң к°ңл§ү](/upload/editor/20241111141025_22E07.jpg)
![[нҸ¬нҶ ] л°•лҜјмҲҳ 2м°ЁкҙҖ, м ңмЈјлҸ„ л°©л¬ёвҖҰмғҒкёүмў…лі‘ м§Җм • нҳ„мһҘм җкІҖ](/upload/editor/20241108102827_ACFD7.jpg)

лҸ…мһҗмқҳкІ¬
мһ‘м„ұмһҗ 비л°ҖлІҲнҳё
0/200