[메디파나뉴스 = 박으뜸 기자] 우리나라는 암묵적으로 ICER(Incremental Cost-Effective Ratio, 점증적 비용-효과비)의 임계값을 '5000만 원'으로 제한해 왔다.
건강보험심사평가원은 ICER의 명시적인 임계값은 사용하지 않으며, 질병의 위중도, 사회적 질병부담, 삶의 질에 미치는 영향, 혁신성 등을 고려한 기존 심의 결과를 참조해 탄력적으로 평가한다고 밝히고 있다.
그러나 그동안의 통계를 살펴봤을 때, 우리나라에서 급여로 평가된 신약 중 ICER 최대값 5000만 원 이상을 넘긴 치료제는 없다.
그러므로 올해는 'ICER 임계값의 현실적인 상향 조정'이 진지하게 논의돼야 한다는 의견이 적지 않다.
해외는 혁신적인 약제의 경우 탄력적으로 ICER 임계값을 적용해 환자의 신약 접근성이 저하되지 않도록 유연한 자세를 취하고 있으나, 우리나라는 아주 오래도록 5000만 원이라는 천장을 깨지 못하고 있다.
이는 심평원이 2022년 12월부터 공개하고 있는 경제성평가 제출 약제의 비용효과성 평가결과(ICER)에서 더욱 확실해진다.
ICER는 효과가 개선된 신약의 경제성을 평가하는 판단 기준으로, 비교 대안에 비해 신약의 증가된 효과 혹은 효용 한 단위 당 소요되는 추가 비용을 나타낸다.
ICER는 특정 임계값과 비교해 그 이하일 경우 신약이 비교대안에 비해 비용효과적인 것으로 해석한다.
ICER 임계값은 1QALY 당 지불 가능한 비용으로, 국가가 수용할 수 있는 ICER 값의 최대치다. QALY는 질 보정수명으로 삶의 양과 질의 변화를 결합한 지표다. 1QALY는 완전한 건강 상태로 1년을 산다는 의미를 가진다.
의약품 선별등재제도 도입 이후 15년간의(2007년~2021년) ICER 값을 살펴보면, 일반약제 28개의 ICER 중앙값은 1579만 원, 항암제 32개는 4516만 원, 희귀질환치료제 12개는 3232만 원이었다.
최대값만 봐도 항암제 4997만 원, 희귀질환치료제 4729만 원으로 5000만 원을 넘긴 치료제는 없었다.
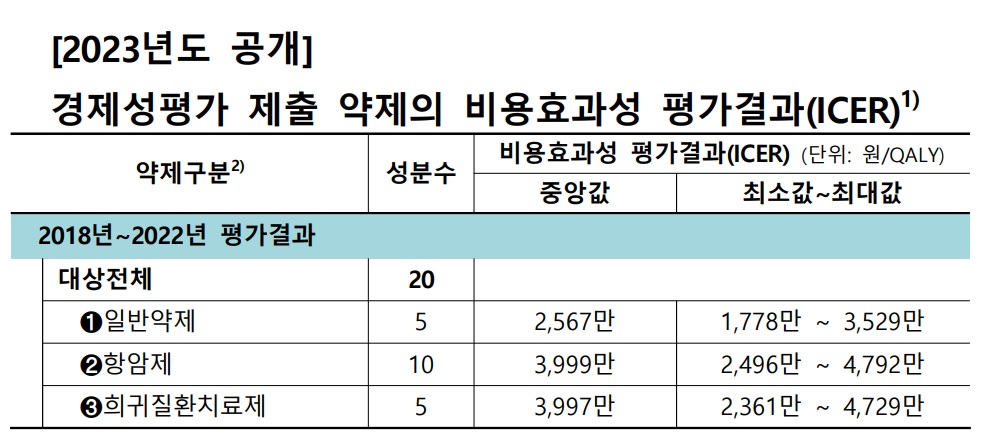
2023년 12월에 공개된 2018년~2022년의 평가 결과도 비슷했다.
일반약제 5개의 ICER 중앙값은 2567만 원, 항암제 10개는 3999만 원, 희귀질환치료제 5개는 3997만 원이었다.
항암제의 최대값은 4792만 원, 희귀질환치료제의 최대값은 4729만 원이었다.
통상적으로 이 ICER 임계값은 1인당 국내총생산(GDP)을 참고하고 있다.
이 가운데 우리나라는 항암제, 희귀질환 치료제의 경우 예외적으로 ICER 임계값을 보통의 신약보다 2배 많은 범위인 2GDP, 1인당 GDP의 2배 수준까지 탄력 적용하고 있다.
문제는 우리나라가 참고한 1인당 GDP가 2013년도 기준의 2500만 원이라는 점이다. 이렇다 보니 지금까지 항암제, 희귀질환의 ICER 임계값은 최대 5000만 원으로 정해져온 것이다.
그런데 지난 2015년 우리나라 1인당 GDP는 이미 3000만 원을 넘어선 상태다. 이렇게 되면 ICER 임계값이 6000만 원으로 상향돼야 하는 것이 맞다.
그럼에도 우리나라는 10년 전 기준에서 벗어나지 못한 채 신약은 ICER 5000만 원에 묶여 평가가 되고 있다.
이에 제약업계는 ICER 임계값이 현실에 맞게 상향돼야 한다는 주장을 지속하고 있다.
실제로 해외에서는 혁신 신약을 평가할 때 GDP를 다른 질환의 2~3배로 설정하는 등 질환의 특성을 고려해 판단하고 있다. 우리나라의 ICER 임계값 범위가 2500만 원~5000만 원 수준이라면, 해외는 5000만 원~1억 원 등으로 훨씬 높은 기준을 정해 신약을 평가한다. 이는 GDP를 감안할 때 우리나라가 다른 국가에 비해 매우 낮은 수준임을 증명하는 대목이다.
일각에서는 과거의 GDP 수준에 묶여 ICER가 낮게 적용된다면 국내 환자들의 신약 접근성이 떨어지는 것은 물론, 한국에 신약 도입을 포기하는 제약사들이 늘어날 것이라 비관적으로 보기도 했다.
결과적으로 우리나라는 'ICER 임계값 현실화'가 요구되고 있다. ICER 값의 상향 조정은 업계 뿐만 아니라 국회에서도 논의를 요구한 사안이다.
다만 우리나라 건강보험 재정 지속 가능성 등을 이유로 지금까지 ICER 임계값의 상향 조정은 이뤄지지 않고 있다.
기술이 발달하면서 생존기간을 급격하게 늘린 신약들은 계속 등장하고 있다. 이들 신약은 높은 효과로 인해 사용량과 약제비도 함께 증가돼 비용효과성 입증이 불리한 상황이다.
따라서 혁신 신약에 대해서 만큼은 '제도적 유연성'을 보여줘야 한다는 주장이 힘을 얻고 있다.
한 가지 희망적인 점은 우리나라도 'ICER 탄력 적용' 가능성이 높게 점쳐지고 있다는 것이다.
최근 정부는 혁신 신약에 대한 적정가치를 인정해주는 약가제도 방안을 발표한 바 있다. 이번 방안은 얼마 전 국무총리 주재로 발족된 바이오헬스혁신위원회의 주요 안건인 '바이오헬스분야 킬러규제 철폐 방안'의 일환이다.
정부는 세 가지 혁신성 인정 요건을 충족하는 약제의 경우 탄력적으로 ICER 임계값을 적용할 방침이다. 이는 혁신성이 인정된 신약에 대한 약가 우대 의지를 범정부 차원에서 표명한 것과 다름없다.
정부가 내놓은 혁신 신약의 기준 요건은 ①대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ②생존기간의 상당 기간 연장 등 임상적으로 의미 있는 개선이 입증된 경우 ③식품의약품안전처에서 신속심사로 허가된 신약(GIFT) 또는 미국 FDA의 획기적의약품지정(BTD), 유럽 EMA의 신속심사(PRIME)로 허가된 경우다.
이 세 가지 요건 모두를 충족하면 ICER 임계값을 탄력적으로 적용받을 수 있을 것으로 전망된다.
정부 발표 후 제약업계는 올해 현실적이고 실질적인 2GDP 수준의 ICER 임계값이 반영될 것이란 기대감을 감추지 않고 있다.














![[현장포토] 2024 건강서울페스티벌 '우리는 당신의 약사입니다'](/upload/editor/20240929135628_03BEE.jpg)
![[현장포토] '바이오플러스-인터펙스 코리아 2024'](/upload/editor/20240710110419_92CF9.jpg)

독자의견
작성자 비밀번호
0/200